第一作者:范梅梅、张志勋
通讯作者:刘广宇、沈震
发表期刊:Antimicrobial Agents and Chemotherapy
期刊5-Year Impact Factor:4.5
通讯单位:浙江省全省医学表观遗传学重点实验室、杭州师范大学基础医学院、上海交通大学医学院附属仁济医院
论文DOI: https://doi.org/10.1128/aac.00671-25
成果简介
2026年2月,杭州师范大学基础医学院刘广宇副教授团队联合上海交通大学医学院附属仁济医院沈震副研究员,在抗菌药物领域权威期刊《Antimicrobial Agents and Chemotherapy》发表题为 “Phylogenetic diversification and fitness trade-offs of TetA variants in mediating eravacycline resistance in Klebsiella pneumoniae” 的研究论文。
该研究对全球 824 株携带tetA基因的肺炎克雷伯菌(tetA-carrying K. pneumoniae, TPKP)进行了系统的流行病学和功能分析,首次识别出28种TetA变体并将其划分为三个进化分支。研究重点发现,TetA-1.6、1.8、1.10和2.6四种变体不仅能介导替加环素耐药,还表现出此前未见报道的“依拉环素(eravacycline)”耐药表型。深入研究揭示了这些“高风险变体(VWPRs)”虽具耐药优势,但在临床和环境中传播受限,其根本原因在于表达这些变体不仅会减缓细菌生长,更显著降低了细菌对临床常用消毒剂H2O2及环境重金属镉(Cd)的耐受力。这一“耐药代价”与生态权衡机制,为解释耐药基因在复杂生态系统中的演变提供了新视角,也为制定基于One Health策略的耐药防控提供了科学依据。
引言
碳青霉烯耐药肺炎克雷伯菌(CRKP)已成为全球公共卫生的严峻威胁。作为应对该类“超级细菌”的最后一道防线,替加环素和依拉环素等新型四环素类药物的应用日益广泛,但随之而来的耐药问题也愈发凸显。尽管已知TetA外排泵是肺炎克雷伯菌产生替加环素耐药的主要驱动因素,但科学界对TetA变体的演化轨迹、全球流行趋势以及它们在传播过程中面临的生态限制依然知之甚少。
我们不禁好奇:这些变体是如何在抗生素压力下不断进化的?为什么某些具有极高耐药性的变体没有在临床中大规模爆发?本研究通过整合大数据挖掘、分子进化分析和功能实验,试图解开TetA变体在“耐药”与“生存”之间的博弈之谜。
图文导读
全球视野:TPKP的流行病学演变
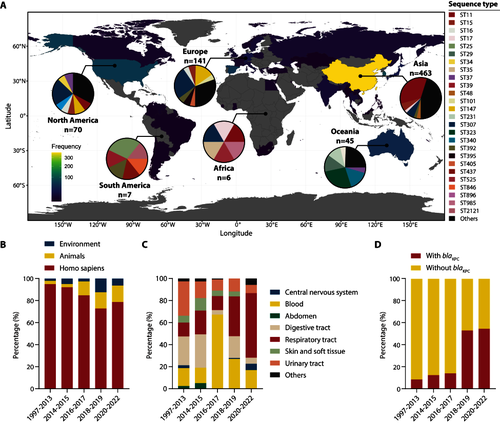
我们分析了1997年2022年间824个TPKP基因组,发现其广泛分布于45个国家,其中亚洲流行率最高(63.5%)(图1A)。从流行趋势看,高风险克隆 ST11 在亚洲占据主导地位,且与blaKPC基因的共存率在近二十年间从9.7% 飙升至55.4%(图1D)。自2015年后,源自环境和动物的TPKP比例显著增加,暗示非人类宿主已成为耐药基因传播的重要温床(图1B)。
图1. 全球产TetA肺炎克雷伯菌(TPKP)的流行病学特征
系统分类:TetA的进化版图
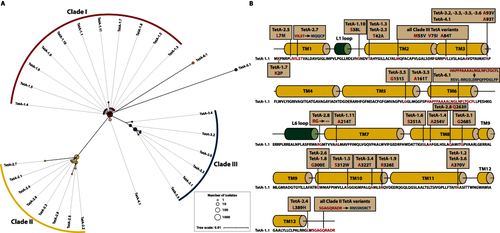
通过对28种变体的系统发育分析,我们将TetA家族划分为三个主要分支(Clade I-III)(图2A)。AlphaFold3预测显示,变体的突变热点主要集中在跨膜结构域 TM3、TM8和TM10,这些区域可能决定了外排泵对药物的识别效率(图2B)。其中最独特的TetA-5.1变体被发现与霍氏肠杆菌密切相关,揭示了跨属水平基因转移的可能性。
图2. TetA变体的系统发育进化树与蛋白质结构突变图谱
质粒动态:驱动耐药扩散的载体
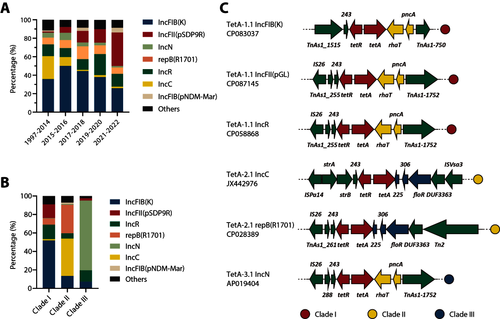
TetA变体的扩散呈现出明显的质粒偏好性。Clade I倾向于随IncFIB(K)质粒传播,而Clade III则与IncN质粒紧密结合。有趣的是,随着时间推移,IncFII(pSDP9R)质粒逐渐取代了旧有的IncC质粒,成为推动TetA扩散的新主流载体。
图3. tetA质粒复制子的流行趋势及其遗传环境分析
功能发现:新型依拉环素耐药表型
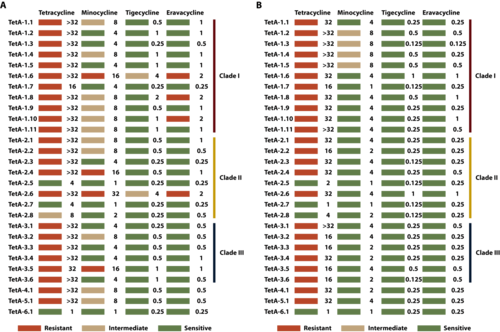
这是本研究的核心发现之一:TetA-1.6、1.8、1.10 和 2.6 变体被确认为高风险变体,它们不仅显著提升了对替加环素的耐药性,还介导了对第四代四环素——依拉环素的交叉耐药(图4)。
图4. 不同TetA变体对四代四环素类抗生素的耐药表型
生态代价:完美的耐药并不存在
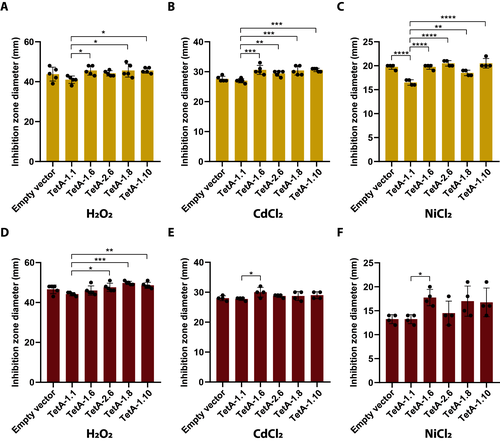
既然这些VWPRs如此强大,为何没有统治世界?实验给出了答案:环境敏感性(图5)。表达VWPRs的菌株对临床常用的H2O2消毒剂表现出极高的敏感性。不仅如此,在重金属镉(Cd)存在的环境下,这些高耐药菌株的生存率大幅下降。这种“生态权衡”意味着:当细菌选择了极端的抗生素耐药性时,它们在医院环境消毒和土壤/水体重金属压力下的适应力便会大打折扣。
图5. 高风险TetA变体对消毒剂和重金属的辅助敏感性
小结
本研究通过One Health视角,揭示了肺炎克雷伯菌TetA变体在进化过程中的增益与代价。这一发现极具临床指导意义:我们可以利用H2O2等消毒手段特异性地杀灭这些高风险耐药株,或者通过监测工业污染区(如重金属超标点)的TPKP 演化,来预判耐药趋势。这一研究再次证明,抗生素耐药性的传播是一场生态“拔河”,每一个进化选择的背后都伴随着生存的博弈。
第一作者简介:
基础医学院硕士研究生范梅梅(左三)、张志勋(右一)为共同第一作者。陈凤(右三)、刘潇蔚(左二)、邓礼勤(左一)、雷艺杰(右二)也为本研究做出了重要贡献。本研究受到国家自然科学基金以及杭州师范大学人才科研启动经费的支持。
通讯作者介绍:
刘广宇,杭州师范大学基础医学院学院副教授(独立PI),硕士生导师。从本科到博士后都在牛津大学完成,获牛津大学威廉邓恩病理学院卓越博士后奖。浙江省科技副总、杭州市海外高层次人才、浙江省微生物学会医学微生物学专委会委员、联川生物高级技术顾问、英国微生物学会会刊《Microbiology》编委、《Military Medical Research》青年编委、《iMeta》青年编委。长期从事的研究领域为“膜蛋白大分子机器介导病原细菌致病与耐药的机制、以及人体菌群的基因编辑与靶向调控”,研究成果发表于EMBO Journal,eLife,Plos Pathogens等高水平期刊。
沈震,医学博士,副研究员,牛津大学访问学者。主要研究方向为临床重要病原菌耐药与致病机制。主持国家自然科学基金3项,并入选上海市“浦江人才”和“青年科技英才扬帆计划”。以第一及通讯作者发表SCI论文20篇,研究成果发表于Drug Resist Updat、Emerg Infect Dis、Emerg Microbes Infect、Clin Microbiol Infect等微生物领域权威期刊。